Ученые обнаружили новый путь для разработки технологий биотоплива
За миллиарды лет практики природа создала самые энергоэффективные машины. Одна из них, NiFe-гидрогеназа, является самой старой среди микроорганизмов и используется для метаболизма водорода. Используя инфракрасную спектроскопию с преобразованием Фурье, исследователи раскрывают путь переноса протона этого фермента, открытие, которое, как ожидается, внесет вклад в создание новых клеток биотоплива.
Несмотря на все открытия, достигнутые технологией на протяжении всей нашей жизни, во многих случаях она отстает от того, что может сделать природа. Муравьи могут нести в 5000 раз больше своего веса, а паутина в пять раз прочнее стали. Топливная эффективность ничем не отличается. В новой работе, исследователи из Нараского института науки и технологии (NAIST) сообщают о новых подробностях пути переноса протонов NiFe-гидрогеназы с использованием инфракрасной спектроскопии с Фурье-переносом (FT-IR). Этот перенос крайне важен для метаболизма водорода микроорганизмами, и исследование дает ученым лучшее понимание того, как имитировать природу в создании новых биотопливных клеток.
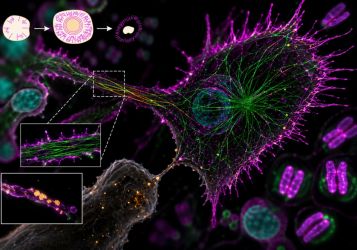
Гидрогеназа - ключевой фермент метаболизма водорода, катализирующий обратимую активацию молекулярного водорода.
Метаболизм водорода является одной из древнейших форм производства энергии для жизни и одной из наиболее интенсивно изучаемых в силу его значимости в эволюции. Этот процесс также привлек внимание, поскольку является чистым источником энергии. Среди ферментов, ответственных за метаболизм водорода, NiFe-гидрогеназа является наиболее распространенной и древнейшей.
Много известно об энзиме. Он обратимо окисляет атомы водорода через свой активный центр Ni-Fe, который окружен определенными аминокислотами. Тем не менее, отмечает профессор NAIST Шун Хирота, руководивший исследованием, необходимо понять некоторые основы химических реакций, прежде чем использовать эту наномашина для разработки технологий биотоплива.
«Гидрид и протон координируются с сайтом Ni-Fe в цикле протонирования-депротонирования, что приводит к четырем состояниям гидрогеназы. Но путь переноса протона остается неизвестным», - говорит он.
Одной из причин отсутствия ясности была неспособность разрешить частоты растяжения различных водородных связей. В новой работе команда Хироты в сотрудничестве с другими исследователями в Японии и Китае решила эту проблему, наблюдая фотопреобразования трех состояний гидрогеназы с помощью ИК-спектров.
Различные частоты поглощения показали, что один из четырех цистеинов, цистеин 546, наряду с другой аминокислотой, глутаминовой кислотой 34 и упорядоченной молекулой воды, являются критическими для переноса. Ученые использовали новую информацию, чтобы сделать вывод, как молекула серы цистеина 546 и кислотная группа в глутаминовой кислоте 34 образуют водородные связи, чтобы регулировать транспорт водорода.
«Наши результаты показывают, что цистеин 546 является донором и акцептором протонов в цикле NiFe-гидрогеназы. Они также демонстрируют, как низкобарьерная водородная связь для глутаминовой кислоты 34 образуется и расщепляется во время каталитического цикла», - отмечает Хирота.
Микроорганизмы приспособились к более широкому диапазону условий окружающей среды, чем люди. Их можно найти в комфортном климате наших спален и в самых агрессивных условиях на земле. Таким образом, видение того, как NiFe-гидрогеназа переносит протоны обеспечивает парадигму для исследователей, стремящихся к производству высокоэффективных энергетических катализаторов в целом ряде условий, пишет ScienceDaily.
«Жизнь потратила миллиарды лет на адаптацию к энергии. Мы считаем, что это дает нам лучшую модель для повышения энергоэффективности в будущем», - говорит Хирота.
































Написать комментарий